isomeria optica
Los isómeros ópticos no se pueden superponer, como ocurre con las manos derecha e izquierda. Presentan las mismas propiedades físicas y químicas pero se diferencian en que desvían el plano de vibración de la
luz polarizada en diferente dirección:
- un isómero desvía la luz polarizada hacia la derecha (en orientación con las manecillas del reloj) y se representa con el signo (+): es el isómero dextrógiro o forma dextro;
- el otro isómero óptico la desvía hacia la izquierda (en orientación contraria con las manecillas del reloj) y se representa con el signo (-)(isómero levógiro o forma levo).15
Otra forma de nombrar estos compuestos es mediante el convenio o
nomenclatura D-L, normalmente empleando la
proyección de Fischer. Esta nomenclatura es absoluta pero no necesariamente la forma (D) coincide con el isómero dextrógiro o forma (+).
16

Formas R y S del bromoclorofluorometano.
También pueden representarse estos isómeros con las letras (R) y (S). Esta
nomenclatura R-S, que sigue las
reglas de Cahn-Ingold-Prelog, también se utiliza para determinar la configuración absoluta de los carbonos quirales.
Así pues, hay tres sistemas de nombrar estos compuestos:
- según la dirección de desviación del plano de la luz polarizada, distinguimos las formas dextro (+) y levo (-);
- según la nomenclatura D-L (Formas D y L), que es inequívoca para isómeros con un solo carbono asimétrico,17 y
- según la configuración absoluta R-S (formas R y S),18 más adecuada para moléculas con varios centros asimétricos.
Diasteroisómeros[editar]
Cuando un compuesto tiene más de un carbono asimétrico, podemos encontrar formas enantiómeras y otras formas que no son exactamente copias especulares, por no tener todos sus carbonos invertidos. A estas formas se les llama
diasteroisómeros. Por ejemplo, el 3-bromo-butan-2-ol posee dos carbonos asimétricos por lo que tiene 4 formas posibles. De ellas, algunas son enantiomorfas, como (2S,3S)-3-bromo-butan-2-ol y (2R,3R)-3-bromo-butan-2-ol. En cambio, (2R,3S)-3-bromo-butan-2-ol es un diastereoisómero de los dos anteriores.
Mezcla racémica y formas meso[editar]

Formas R y S del ácido láctico. Enantiómeros del
ácido láctico o ácido 2-hidroxipropanoico.
Una
mezcla racémica es la mezcla equimolecular de los isómeros dextro y levo. Esta fórmula es ópticamente inactiva (no desvía el plano de la luz polarizada). La mezcla de ácido D-láctico y L-láctico forma una mezcla racémica, ópticamente inactiva.
Si un compuesto posee dos carbonos asimétricos, puede tener uno dextrógiro y otro levógiro, pero si tiene un plano de simetría, en conjunto se comporta como ópticamente inactivo y recibe el nombre de
forma meso. Es el caso del
ácido tartárico o 2,3-dihidroxibutanodioico, uno de cuyos isómeros es una forma meso.
Poder rotatorio específico[editar]
Es la desviación que sufre el plano de polarización al atravesar la luz polarizada una disolución con una
concentración de 1 gramo de sustancia por cm³ en un recipiente de 1 dm de altura. Es el mismo para ambos
enantiómeros, aunque de signo contrario. Se mide con el
polarímetro.
19



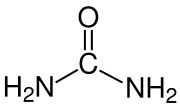











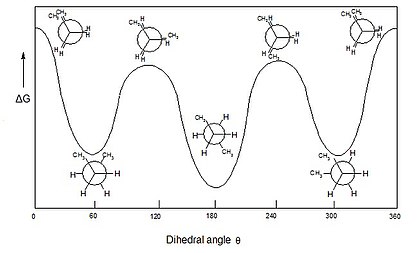

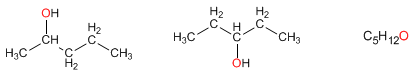
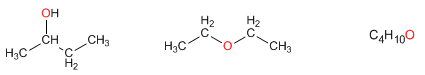
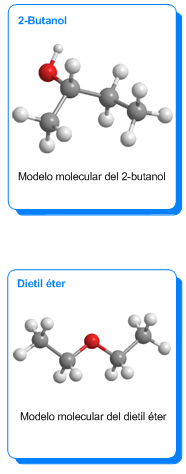 Definición de isómeros
Definición de isómeros